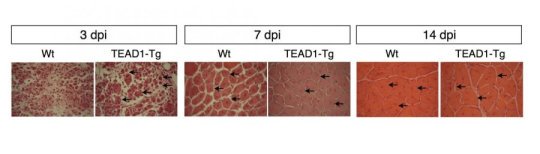
Hình: Sự khác biệt giữa các bó cơ bình thường và bó cơ của chuột biến đổi gen. Các bó cơ bình thường được trình bày ở hình bên trái tương ứng với các mốc thời gian 3, 7 và 14 ngày sau khi tổn thương. Các bó cơ trong hình bên phải được lấy từ chuột biến đổi gen, biểu hiện vượt mức gen TEAD1, làm tăng đáng kể tế bào gốc cơ. Các điểm màu đỏ và mũi tên trên hình chỉ vị trí của tế bào gốc cơ.
Các vận động viên, người già và những người bị bệnh thoái hóa cơ được lợi từ các liệu pháp đẩy mạnh phục hồi hệ cơ. Khi hệ cơ kết nối với xương bị tổn thương, các tế bào gốc cơ được đánh thức từ trạng thái không hoạt động trở thành dạng hoạt động và sửa chữa các sai hỏng đó. Tuy nhiên, khi cơ già đi, số lượng và chức năng của tế bào gốc suy giảm ảnh hưởng đến chức năng và khả năng tái tạo của mô cơ. Nhóm nghiên cứu của Carnegie’s Christoph Lepper, bao gồm các nhà nghiên cứu từ Đại học Missouri, nghiên cứu về kích thước của “ổ” tế bào gốc cơ. Họ tự hỏi nếu số lượng tế bào gốc có thể tăng lên và điều này có liên quan đến bất kì lợi ích nào về chức năng của cơ không?
Bằng cách sử dụng chuột biến đổi gen, các nhà khoa học thấy rằng trong khi kích thước bó cơ không thay đổi, điều đáng ngạc nhiên là nó có khả năng chứa một số lượng lớn tế bào gốc hơn những gì chúng ta nghĩ trước đây. Số lượng tế bào gốc khổng lồ đó có thể giúp phục hồi các tổn thương của cơ và nhanh hơn thời điểm chỉ có một số lượng bình thường tế bào gốc cơ. Đội ngũ nghiên cứu cũng thấy rằng việc tăng tế bào gốc làm giảm nguy cơ thoái hóa, suy yếu cơ, điều này có khả năng mang lại lợi ích trong việc chống lại căn bệnh teo cơ. Nghiên cứu này được công bố ngày 11 tháng 10 năm 2016 trên tạp chí eLife.
Tế bào gốc cơ, hay còn gọi là các tế bào vệ tinh (satellite cell), là những tế bào cơ chưa biệt hóa giúp đẩy mạnh sự tăng trưởng, hồi phục và tái tạo cơ. Lepper giải thích rằng những tế bào vệ tinh này tạo nên 5-7% của tất cả các tế bào cơ và rất cần thiết cho việc tái tạo cơ bắp. Khi chuột sinh ra, các tế bào vệ tinh này phân chia và biệt hóa khoảng 3-4 tuần dẫn đến sự tăng trưởng mô. Sau đó, chúng trở về trạng thái im lặng đến khi phát hiện một chấn thương của cơ thể. Số lượng tế bào vệ tinh tồn tại vào thời điểm này tương đối ổn định với kích thước mô cơ của vật chủ. Nhóm nghiên cứu muốn xem liệu tỉ lệ này có thể được thao tác và nếu như vậy, liệu có gây ra bất kì hậu quả lên sinh lý của cơ thể hay không?
Richard Tsika, cộng sự của Lepper đã tạo ra chuột biểu hiện vượt mức gen TEAD1 và thấy rằng protein được tạo ra từ gen này, tác động đến sự điều hòa của một loại bó cơ. Chuột chuyển gen TEAD1 tăng gấp 6 lần số lượng tế bào vệ tinh so với bó cơ không biểu hiện TEAD1 trên tất cả các nhóm cơ được phân tích.
Điều ngạc nhiên là nghiên cứu này phát hiện ra rằng các bó cơ có thể “liên kết” với các tế bào gốc của nó và ảnh hưởng đến kích thước của “ổ” tế bào gốc. Sự kết nối phân tử đến các tế bào vệ tinh là nguồn gốc của sự gia tăng tế bào gốc.
Các nhà nghiên cứu đề xuất rằng việc tăng số lượng tế bào vệ tinh, không có bất kì thay đổi với toàn bộ kích thước bó cơ, làm cho mô hình chuột biến đổi gen TEAD1 như một sinh vật mô hình tốt. Với nó, các nhà khoa học hi vọng sẽ khám phá các dòng thác phân tử giúp điều hòa số lượng tế bào gốc cơ và các tín hiệu “dừng” và “đi” gây ra sự biệt hóa và im lặng của tế bào.
Kiều Oanh
Theo Science Daily






